https://mp.weixin.qq.com/s/LwVi4VDxS0rKYHV5XYowbA
人類的許多疾病都是由細菌感染引起的,如敗血症、細菌性皮膚感染和各種細菌性呼吸道感染等,大多數都可以用抗生素進行治療。然而,隨著抗生素耐藥菌株的出現,抗生素的療效減弱。此外,傳統的抗感染治療總是注重細菌的殺滅,而常常忽視內毒素的清除。實際上,革蘭氏陰性菌在細胞生長、裂解或抗生素治療過程中釋放的內毒素,是引起發熱、中風、器官衰竭甚至死亡的關鍵原因。用抗內毒素抗體和內毒素中和蛋白隔離和中和迴圈內毒素是關鍵的治療選擇。因此,越來越多的中和治療藥物包括抗內毒素抗體和內毒素中和蛋白用於中和體內的內毒素。雖然,所有內毒素都有一個共同的結構基元,但不同細菌種類的內毒素結構基序差異很大,這將降低現有內毒素中和劑的結合力和清除效率。
此外,中和治療藥物與宿主細胞在識別和結合有害細菌和內毒素方面存在競爭關係。為了提高抗細菌感染效率,需要具有高親和力的中和治療藥物進行競爭性吸附和中和細菌和內毒素,有效預防或抑制宿主細胞感染。
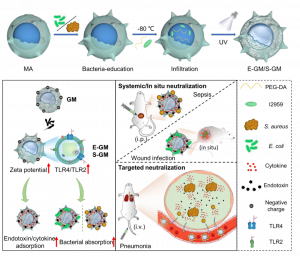
鑒於此,澳門大學王瑞兵團隊構建了具有完整膜結構的胞內凝膠巨噬細胞,即巨噬細胞海綿,通過受體-配體相互作用中和細菌和內毒素,緩解細菌感染症狀。此外,研究團隊還發現細菌感染的巨噬細胞可以上調細胞膜病原體相關受體,並增加降低細胞膜的電負性,經過胞內凝膠化後明顯增強巨噬細胞海綿對細菌和內毒素的識別清除。
巨噬細胞海綿構建及內毒素中和作用
本研究的目的是開發一種廣譜型中和試劑用於細菌感染性疾病的治療。為了實現這一目標,我們首先將水凝膠的製備轉移到細胞質中,採用低溫冷凍-常溫解凍方式使凝膠材料滲入胞內構建凝膠化巨噬細胞(巨噬細胞海綿),並確認其細胞形態與宿主巨噬細胞類似,證實其膜結構和膜蛋白與宿主巨噬細胞保持一致。在體外抗菌感染治療方面,考察了其吸附清除細菌、內毒素和炎症因數的性能。
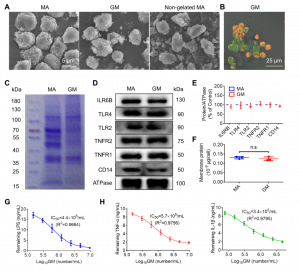
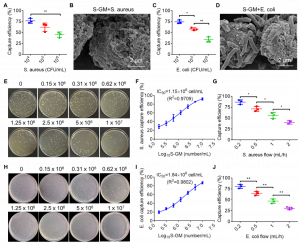
細菌誘導預處理增強巨噬細胞海綿細菌捕獲能力
在胞內膠凝前,對巨噬細胞進行細菌誘導處理,分析其細胞膜表面病原體相關蛋白受體表達的變化,測定其細胞膜電位。採用掃描電鏡分析巨噬細胞海綿和細菌的表面吸附情況,並利用共聚焦顯微鏡驗證巨噬細胞海綿對細菌的靜態捕獲性能,測定細菌清除效率。為類比血流情況的細菌捕獲效果,採用微流控晶片技術證實巨噬細胞海綿對細菌的動態捕獲性能,並測定細菌清除效率。證實經細菌誘導預處理的巨噬細胞海綿對革蘭氏陰性菌和革蘭氏陽性菌均顯示出較強的靜態和動態捕獲能力。
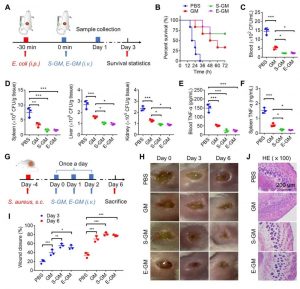
抗敗血症和細菌傷口感染治療
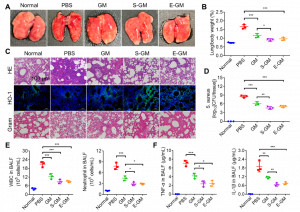
在敗血症小鼠模型中,經細菌誘導處理的巨噬細胞海綿可提高小鼠存活率,腎臟和肝臟中細菌數量顯著降低,同時炎症細胞因數TNF-α水準也下降。這主要歸因於巨噬細胞海綿表面TLR4-LPS結合作用,有利於吸附和清除大腸桿菌和促炎細胞因數。除全身細菌感染外,還評估了巨噬細胞海綿對細菌感染性傷口的治療效果。與革蘭氏陰性菌(大腸桿菌)誘導的膿毒症模型不同,這裡給小鼠皮下接種革蘭氏陽性菌(金黃色葡萄球菌)。結果顯示巨噬細胞海綿加速了傷口癒合過程。HE染色進一步證實,巨噬細胞海綿減少了創面皮膚中的炎症細胞浸潤、成纖維細胞遷移和增殖。傷口皮膚中的細菌含量也降低至較低水準。值得注意的是,在大腸桿菌誘導的膿毒症模型中,經大腸桿菌預處理的巨噬細胞海綿在降低器官細菌數量和全身炎症水準方面,表現出比經金葡菌預處理的巨噬細胞海綿更高的效率,而在鼠感染金黃色葡萄球菌傷口模型中,經金葡菌預處理的巨噬細胞海綿對傷口癒合表現出更好的治療效果。
抗細菌性肺炎靶向治療
凝膠化巨噬細胞與LPS誘導的炎性肺泡細胞共孵育,利用共聚焦顯微鏡觀察其特異性吸附結合情況。採取LPS霧化吸入法構建小鼠急性肺炎模型,經尾靜脈給予螢光標記的凝膠化巨噬細胞,利用共聚焦螢光成像分析心、肝、脾、肺、腎的螢光強度分佈,進一步開展肺組織切片螢光成像,分析凝膠化巨噬細胞在肺組織中的增強滲透情況。小鼠經過巨噬細胞海綿治療後,分析肺組織幹濕比,利用試劑盒測定肺組織MPO和MDA含量,開展肺組織病理切片分析(HE染色和HO-1染色),檢測肺灌洗液和血清的炎症因數水準(TNF-α和IL-1β),開展肺組織中M1型巨噬細胞的免疫螢光成像和流式細胞術定量分析。證實經細菌誘導預處理的巨噬細胞海綿可靶向富集到肺炎組織,並有效改善細菌感染性肺炎症狀。
總結和展望
具有高穩定性的細胞內水凝膠可以作為理想的細胞質骨架來維持完整的細胞形態,通過巨噬細胞的胞內膠凝直接構建天然中和治療藥物(巨噬細胞海綿),用以吸附和清除細菌、內毒素和細胞因數。在治療應用中,巨噬細胞海綿需要與宿主巨噬細胞競爭結合這些有害物質,但它們都具有相同的膜結構,對細菌和內毒素表現出相似的結合力,這可能導致有害物質的不完全中和。該研究發現對巨噬細胞進行細菌誘導預處理,可增強病原體相關受體(TLR4和LTR2)的產生,並減低巨噬細胞膜的電負性,從而增強巨噬細胞海綿對革蘭氏陰性菌和革蘭氏陽性菌、內毒素和炎症因數的結合力。因此,與宿主巨噬細胞相比,細菌誘導預處理使巨噬細胞海綿在中和細菌和內毒素方面表現出明顯競爭優勢,並且在敗血症、傷口細菌感染和細菌性肺炎治療中顯示出增強療效。這項研究通過巨噬細胞的細菌誘導預處理和隨後的胞內膠凝過程構建巨噬細胞海綿平臺,可以為廣譜細菌感染治療提供全面且有效的中和試劑。
▌論文標題:
A bacterially engineered macrophage sponge as a neutralization decoy to treat bacterial infection
▌論文網址:https://www.cell.com/matter/fulltext/S2590-2385(23)00462-9