疫苗是史上最成功的醫學發明之一。對於免疫原性較低的抗原,佐劑或可增強免疫回應,其機制之一是啟動免疫細胞的模式識別受體(PRRs),進而啟動一系列的免疫應答,促進抗體和細胞因數的產生。多種糖類分子,作為微生物表面的重要信號,可有效啟動PRRs,從而具有作為佐劑材料的潛力。闡明這些糖分子的免疫調節機制,將對指導未來疫苗佐劑的設計提供理論基礎。澳門大學王春明教授、母若雨博士,與南京大學董磊教授在Cell Press細胞出版社期刊Trends in Immunology發表綜述論文,總結了基於糖類佐劑的最新發展趨勢,著重討論了多糖、寡糖或糖聚合物的物理化學特性——包括分子大小、組裝狀態、單糖成分和官能團模式等——如何影響抗原呈遞與免疫應答的過程。
微生物來源的糖類給疫苗佐劑設計帶來了靈感
雖然佐劑已經廣泛應用于現代疫苗開發,但即使是最經典的鋁基佐劑和廣泛使用的佐劑系統04 (AS04),其作用機制仍不夠清晰。隨著對先天免疫系統認識的不斷加深,逐漸發現Toll樣受體(TLRs)、C型凝集素受體(CLRs)和NOD樣受體(NLRs)等PRRs通過識別微生物的病原體相關分子模式(PAMPs),觸發胞內信號,啟動免疫回應。因此可以通過類比病原微生物表面的PAMPs的結構來設計PRRs激動劑。糖類分子是許多病原微生物PAMPs的組成部分。例如,細菌PAMPs:脂多糖(LPS)和肽聚糖(PGN);真菌PAMPs:β-葡聚糖和甘露聚糖,均可刺激一些PRRs,例TLR4和Dectin-1,表現出佐劑活性。儘管目前基於糖類佐劑的研究不斷增多,但其結構複雜性、合成難度高、研究技術缺乏等挑戰阻礙了對糖類潛在佐劑活性的分子基礎的探索。
影響糖類分子與PRRs相互作用的關鍵因素
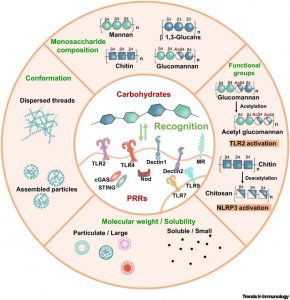
影響糖類分子的生物活性及其識別和啟動PRRs的決定性因素有很多,包括分子品質、溶解度、單糖組成、官能團取代度等(圖1)。
1.分子量/可溶性
分子量大小是所有聚合物的基本特徵,包括多糖。早期研究發現,只有大分子量顆粒型多糖才具有免疫啟動作用。例如,可溶性和不可溶性的真菌多糖均可以結合Dectin受體,但是只有後者能誘導有效的受體聚集和啟動。然而最新研究表明,可溶性(~20 nm)的白色念珠菌來源的甘露聚糖注射到小鼠背部皮下後,不誘導外周免疫反應,但可直接進入引流淋巴結(dLNs),啟動淋巴結先天免疫回應。這一發現可能為佐劑設計和疫苗開發提供一個新思路。
2.官能團及單糖組成
糖類的官能團模式也影響其與PRRs的識別。例如,由幾丁質去乙醯化得到的殼聚糖可以通過啟動NLRP3炎症小體,啟動巨噬細胞免疫回應,而原本幾丁質沒有這種活性。此外,果膠與TLR2-1之間的識別除了受甲酯化修飾程度的調控外,還依賴甲基酯的分佈。一項臨床試驗發現乙醯基也會影響果膠的生物學功能:O -乙醯化果膠可在健康志願者體內有效誘導IgG的產生,但不會引發嚴重的疫苗相關不良反應。
多糖中的單糖結構也影響其與PRRs之間的精確相互作用。之前認為DC-SIGN和L-SIGN,作為密切相關的CLR,它們識別的單糖組成結構是類似的。但最新的研究發現,相較於DC-SIGN,L-SIGN與N -甘露聚糖具有更高的結合親和力。
3.高級構象
糖類一級結構的改變會影響其高級構象,也會影響其與PRRs的識別。例如,乙醯化可改變葡甘聚糖的親疏水性。隨著修飾度的增加,乙醯化葡甘聚糖的結構可以從線性轉變成顆粒狀,並在當乙醯基的修飾度達到1.8時形成較為均一的200-300納米大小的顆粒,可通過特異性啟動巨噬細胞表面的TLR2,啟動免疫回應。此發現表明精細調控糖分子組裝而成的三維形態有助於產生生物活性。
4.與其他PRRs激動劑協同作用
糖類不僅可以單獨作為免疫激動劑,還可與其他PRRs激動劑協同作用。例如一種新型佐劑p(Man-TLR7),是由甘露糖和TLR7激動劑組成的共聚物。它通過識別甘露糖受體(MR)促進樹突狀細胞(DCs)的攝取,並在細胞內啟動TLR7促進DC活化,從而實現MR與TLR7之間的協同作用。此外,多糖自身也可誘導不同PRRs之間的協同合作。有研究發現葡甘聚糖可同時啟動TLR4和MR。以上的發現提示我們在佐劑設計中可以考慮糖類對PRRs的協同作用。
糖類為基礎的PRRs激動劑作為疫苗佐劑調控免疫回應的方式
基於糖類的PRRs激動劑參與調節免疫應答的方式主要通過以下三個方面:(1)抗原運輸途徑(圖2);(2)抗原攝取和呈遞(圖3);(3)適應性免疫應答(圖4)。
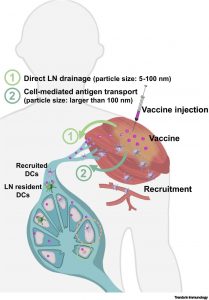
1.調控抗原運輸途徑
一般疫苗是經皮下或肌肉注射,在次級淋巴器官產生適應性免疫應答。因此佐劑的作用是在注射部位誘導局部免疫環境產生趨化因數,招募抗原提呈細胞(APCs),啟動細胞介導的抗原轉運,將抗原運輸到dLNs。然而,某些病毒、納米顆粒或可溶性蛋白可直接通過淋巴管進入淋巴結中,啟動淋巴結中的巨噬細胞、DCs或B細胞。有研究發現直徑5 ~ 100 nm的納米顆粒可以通過淋巴管運輸到淋巴結中,大於100 nm的顆粒可能被困在注射部位的細胞外基質中,需經APCs吞噬處理後才能遷移至LNs,小於5 nm的顆粒會通過血液內皮基底膜擴散,直接進入迴圈。因此可以通過調控疫苗輸送系統的大小來調節抗原運輸的路徑,從而獲得不同的免疫效果。
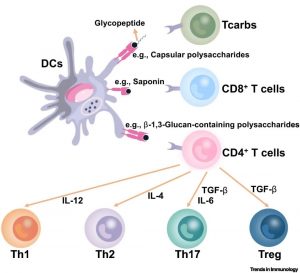
2.調控抗原攝取及抗原呈遞的方式
T細胞免疫應答的啟動依賴於APCs對抗原的攝取和呈遞。抗原被APCs攝取後,在溶酶體中被降解成多肽,裝載在MHC II分子上並運輸到細胞表面啟動CD4+ T輔助細胞。此外,被攝取的外源性抗原可能出現溶酶體逃逸現象,由MHC I分子呈遞,誘導CD8+ T細胞應答,稱為交叉呈遞。一些基於糖類的佐劑可以調節抗原呈遞的方式。例如,基於皂苷的佐劑(SBAs)可在細胞內形成脂質體(LBs),並通過PKR樣內質網激酶(PERK)通路實現外源性抗原的交叉呈遞。此外,還有一項有趣的研究發現,不僅肽段可以由APCs呈遞給T細胞,糖綴合疫苗的多糖成分也可以由MHC II呈遞並啟動糖類特異性CD4+ T細胞(Tcarbs)。
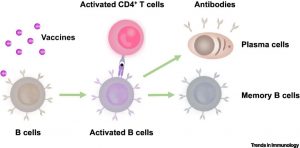
3.調控適應性免疫應答
基於糖類的佐劑還可參與調控適應性免疫應答。例如,一種基於菊粉的多糖佐劑,可同時有效地誘導Th1和Th17免疫反應。類似地,殼聚糖也可有效的誘導Th1免疫應答。同時還發現,多糖結構也會影響適應性免疫應答的類型。例如,酵母細胞表面含有β-1,3-葡聚糖的多糖可以誘導DCs分泌IFN-γ,促進Th1細胞分化。而另外一種甘露聚糖/β-1,6-葡聚糖(MGCP)多糖成分,誘導小鼠naive CD4+ T細胞向調節性T細胞(Treg)分化。此外,基於糖類的激動劑還可直接作用於B細胞(也表達PRRs)並觸發體液免疫。有研究發現,殼寡糖(COS)可直接通過啟動草魚脾臟IgM+ B細胞的MR和整合素,誘導B細胞增殖和分化。
王春明,現任澳門大學中華醫藥研究院和健康科學學院藥物科學系教授,主要研究促進組織修復再生的生物活性材料與細胞治療方法,主持國家自然科學基金委優秀青年科學基金(港澳)、澳門重點研發計畫、澳門科技發展基金-國家自然科學基金委聯合資助等科研專案。王春明的澳門大學個人主頁:https://sklqrcm.um.edu.mo/chun-ming-wang/